Ein neues Verfahren sagt den Krankheitsverlauf von HPV-negativen Kopf-Hals-Tumoren nach der Strahlenchemotherapie vorher. Laut einer aktuellen Studie im Fachjournal „Clinical Cancer Research“ können fünf microRNAs (miRNAs) den entscheidenden Hinweis geben. Die Arbeit entstand am Helmholtz Zentrum München, am Klinikum der Ludwig-Maximilians-Universität München (LMU) und in enger Kooperation mit dem Deutschen Krebskonsortium (DKTK), so eine Pressemeldung auf idw online.
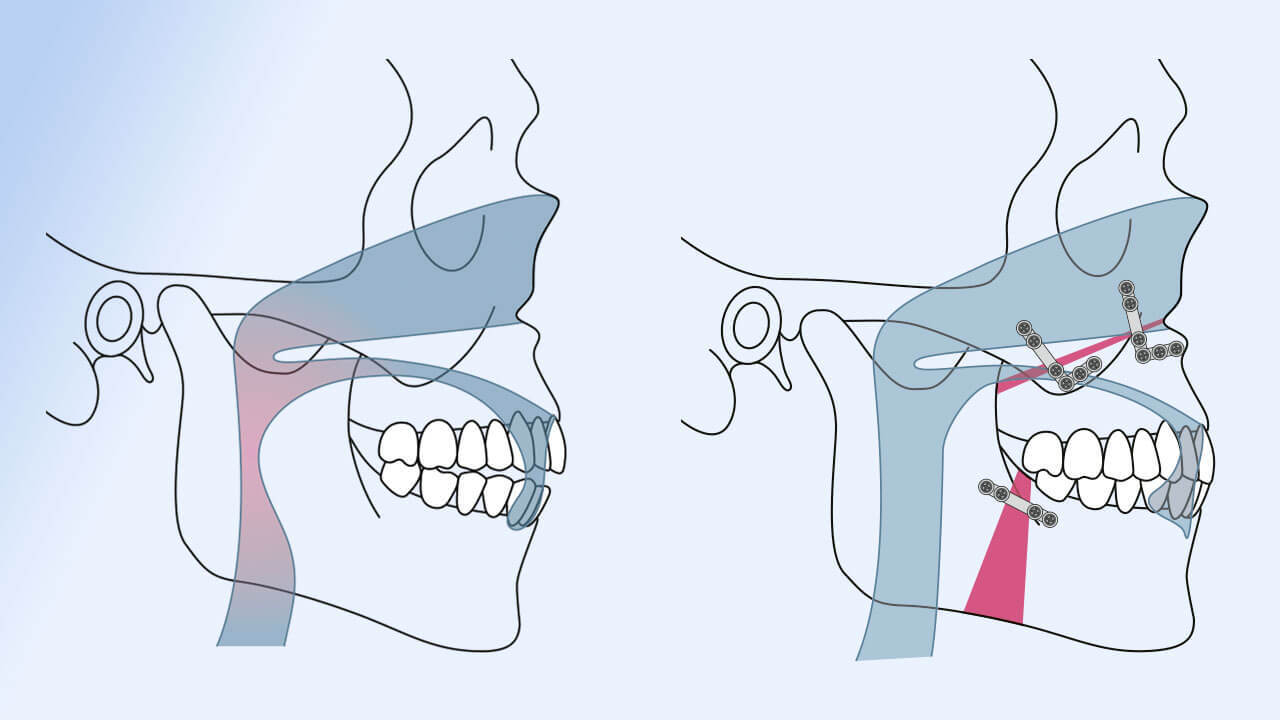
Sogenannte Plattenepithelkarzinome im Kopf-Hals-Bereich werden größtenteils erst in einem fortgeschrittenen Stadium entdeckt und haben meist eine entsprechend schlechte Prognose. Ursache können auch humane Papillomviren (HPV) sein, Hauptursache sind aber das Tabakrauchen und der übermäßige Konsum von hochprozentigem Alkohol.
„Während sich die viral verursachten Tumoren relativ gut behandeln lassen, haben die übrigen Kopf-Hals-Tumoren eine eher schlechte Prognose“, erklärt Prof. Dr. Claus Belka, Leiter der Klinischen Kooperationsgruppe (KKG) Personalisierte Radiotherapie bei Kopf-Hals-Tumoren. Die KKG vereint Wissenschaftler des Helmholtz Zentrums München und der LMU und ist dadurch eng an das DKTK angebunden. „In der vorliegenden Arbeit haben wir untersucht, inwiefern sich anhand molekularer Marker Untergruppen definieren lassen, die nach Strahlenchemotherapie einen unterschiedlichen Krankheitsverlauf nehmen“, so Belka weiter. Das könne eine Möglichkeit zur personalisierten Behandlung bieten. „Für die Etablierung solcher molekularen Marker, die eine Stratifizierung der Patienten erlauben, bietet die Abteilung Strahlenzytogenetik am Helmholtz Zentrum München unter der Leitung von Prof. Horst Zitzelsberger aufgrund der dort verfügbaren Nachweisverfahren die optimale Expertise.“
Ansatz zur personalisierten Therapie
In der aktuellen Studie untersuchten die Forschenden Krebsgewebe aus zwei unabhängigen Probensammlungen: Ein multizentrisches Patientenkollektiv der DKTK Radiation Oncology Group (DKTK-ROG; Koordinator der miRNA-Studie Prof. Michael Henke) sowie ein monozentrisches Patientenkollektiv aus der Klinik für Strahlentherapie und Radioonkologie der LMU (Leitung Prof. Belka). Bei den Analysen konzentrierten sich die Forscher auf sogenannte miRNAs: Winzige Moleküle, die die Aktivität zahlreicher (zum Teil krebsrelevanter) Gene beeinflussen. „Durch die Zusammenarbeit mit den Kollegen konnten wir so insgesamt 162 Proben von Patienten mit HPV-negativen Kopf-Hals-Tumoren untersuchen “, beschreibt Dr. Julia Heß. Sie teilt sich die Erstautorenschaft mit Dr. Kristian Unger, der wie Heß eine Arbeitsgruppe in der Abteilung Strahlenzytogenetik leitet. Aus sämtlichen miRNAs konnten die Forscher fünf herausarbeiten, deren Ausprägung den Krankheitsverlauf und das Rückfallrisiko vorhersagte. „Diese fünf miRNAs – im Fachjargon Signatur genannt – erlauben in Kombination mit weiteren klinischen Werten die Definition von vier Gruppen mit unterschiedlicher Prognose“, ergänzt Unger.
Patienten mit niedrigem Risiko brauchen geringere Intensität
„Solche molekularen Marker sind die erste Voraussetzung für personalisierte Behandlungsansätze bei HPV-negativen Kopf-Hals-Tumoren“, so Studienleiter Belka abschließend. „Wenn sich diese Zahlen im großen Maßstab bestätigen, könnte man daraus künftig personalisierte Anpassungen der Therapieintensität ableiten.“ So wäre es denkbar, bei Patienten mit niedrigem Rückfallrisiko die Intensität zu reduzieren oder bei Hochrisikopatienten diese zu erhöhen. Zudem könne man nun nach den Genen suchen, die von den fünf miRNAs beeinflusst werden und herausfinden, ob sie lohnende Zielstrukturen für die Therapie darstellen.
Hintergrund:
2016 hatten die Wissenschaftler bereits eine miRNA-Signatur gefunden, die den Krankheitsverlauf bei Hirntumoren leichter abschätzbar macht. miRNAs oder microRNAs sind eine Klasse von Molekülen, die aus kurzen Abfolgen von RNA-Bausteinen bestehen. Anders als bei der Proteinsynthese wird die RNA aber hier nicht für den Aufbau von Molekülen benötigt. Im Gegenteil: viele miRNAs sind in der Lage, den Aufbau von bestimmten Proteinen zu verhindern indem sie die entsprechende Bauplan-RNA abbauen. Schätzungen zufolge sind aktuell etwa 2.000 verschiedene miRNAs bekannt.