Wissenschaftler:innen des Helmholtz-Instituts für RNA-basierte Infektionsforschung (HIRI) und des Instituts für Molekulare Infektionsbiologie (IMIB) in Würzburg wollen besser verstehen, wie genau der Mundhöhlenkeim Fusobacterium nucleatum mit verschiedenen Krebserkrankungen in Verbindung steht. Um den molekularen Strategien dieser Bakterien auf die Schliche zu kommen, hat das Team neue genetische Werkzeuge entwickelt. Entdeckt wurde damit ein möglicher Regulator für das Anhaften der Mikroorganismen an Tumorzellen. Die Erkenntnisse dienen der Suche nach neuen therapeutischen Angriffspunkten und wurden kürzlich in dem Fachmagazin PNAS (The Proceedings of the National Academy of Sciences) veröffentlicht.
Fusobakterien neigen zu Tumorgewebe
Mehr als 4.500 Bakterienarten besiedeln den Menschen. Obwohl ihre Bedeutung für Wohlbefinden und Gesundheit ebenso wie für Erkrankungen zunehmend erkannt wird, sind die zugrunde liegenden molekularbiologischen Zusammenhänge zum größten Teil noch unbekannt. Das gilt auch für Fusobakterien: Sie sind häufig in der Mundflora anzutreffen, können jedoch auch andere Stellen des menschlichen Körpers besiedeln, insbesondere Krebsgewebe. Dort fördern sie Tumorwachstum und Metastasen, erschweren die Behandlung und verschlechtern die Prognose. Diese Verbindung ist bereits vielfach bei Darm- und Brustkrebs nachgewiesen worden. Darüber hinaus stehen Fusobakterien zunehmend in Verdacht, auch bei Krebserkrankungen anderer Organe, etwa der Speiseröhre und Bauchspeicheldrüse, eine entsprechende Rolle zu spielen.
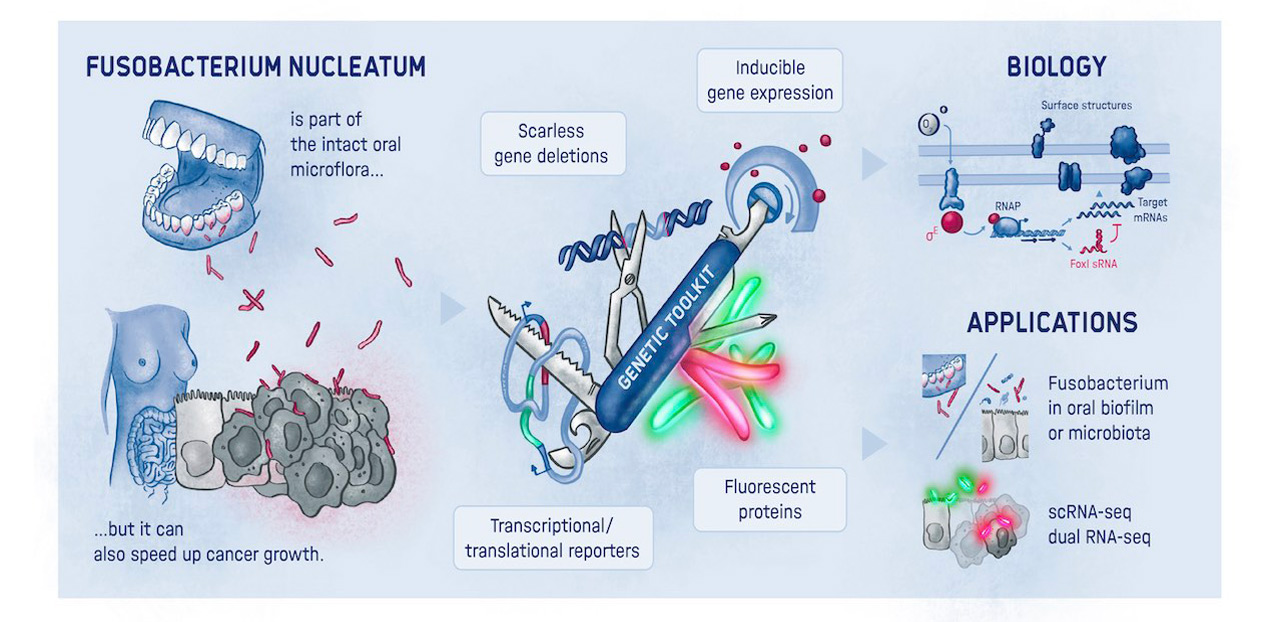
Auf der Fährte eines Anpassungskünstlers
„Fusobakterien sind klinisch höchst relevant, aber selbst noch wenig erforscht“, stellt Jörg Vogel fest. Fusobacterium nucleatum ist ein Bakterienstamm, der sich im Laufe der Evolution früh von anderen bekannten Bakterien wie Escherichia coli (E. coli) entfernt hat. Wissenschaftliche Erkenntnisse, die für den gut erforschten Modellorganismus E. coli gelten, können somit nicht notwendigerweise auf den Mundhöhlenkeim übertragen werden. Ebenso bedarf es neuer genetischer Werkzeuge, um dem Geheimnis der Fusobakterien auf die Spur zu kommen. Die bisherige Forschung konzentrierte sich vor allem auf den Wirt.
Genau hier setzen die Würzburger Wissenschaftler:innen an. „Wir haben ein dringend benötigtes Instrumentarium für den Einsatz in Fusobacterium nucleatum entwickelt und erstmals auch ein Fluoreszenz-Bildgebungsverfahren etabliert, mit dem wir die Mikroorganismen darstellen und verfolgen können“, erläutert Falk Ponath, Erstautor der kürzlich in dem Fachmagazin PNAS (The Proceedings of the National Academy of Sciences) erschienenen Studie. Mithilfe ihrer genetischen Werkzeuge hat das Team einen Faktor entdeckt, der womöglich zur Kontrolle der Adhäsion der Onkomikroben an Tumorzellen beiträgt.
Ponath: „Eine vorangegangenen Untersuchung zeigte, dass eine kleine regulatorische Ribonukleinsäure, sogenannte sRNA, ein Protein der äußeren bakteriellen Zellmembran reguliert. Jetzt konnten wir diesen Mechanismus genauer analysieren und einen beteiligten spezifischen Anpassungsfaktor finden, der verschiedene Proteine der Zellhülle unterdrückt.“ Dieser Anpassungsfaktor zeigte sich unempfindlich gegenüber äußeren Stressoren, reagierte jedoch stark auf Sauerstoff. Das Gas aktivierte den Anpassungsfaktor, der wiederum die sRNA hochfuhr.
Anpassungsfaktor reagiert auf Sauerstoff
Das bereits von anderen Mikroben wie E. coli bekannte Regulierungsprinzip auch in Fusobacterium nucleatum nachweisen zu können, sei vor dem Hintergrund der evolutionären Distanz durchaus überraschend, so Ponath. Zugleich sei es verlockend zu spekulieren, dass der Anpassungsfaktor wie ein Sensor für die Bakterienumgebung fungiere und, vermittelt durch Sauerstoff, die Zellhülle umgestalte.
Fusobakterien nutzen die Proteine ihrer Zellhülle für die Interaktion mit dem Wirt. Ob jedoch die beschriebenen Prozesse ursächlich dafür sind, dass der Mundhöhlenkeim Tumorgewebe besiedelt, muss noch weiter untersucht werden.
Ponath F, Zhu Y, Cosi V, Vogel J (2022) Expanding the genetic toolkit helps dissect a global stress response in the early-branching species Fusobacterium nucleatum. The Proceedings of the National Academy of Sciences (PNAS). DOI: 10.1073/pnas.2201460119