Bakteriophagen sind spezielle Viren, die ausschließlich Bakterien angreifen und deshalb eine Alternative zu Antibiotika darstellen können. Allerdings ist es aufwendig, die für ein bestimmtes Bakterium wirkenden Phagen zu identifizieren und zu gewinnen oder gar standardisiert herzustellen. Daher wird die Phagentherapie in Deutschland nur als individueller Heilversuch eingesetzt. Ein Team aus österreichischen, deutschen und schweizerischen Forschern konnte nun erstmals zeigen, dass gezielt herangezüchtete Phagen deutlich besser gegen multiresistente Keime wirken, als bekannte Wildtypen. Die Ergebnisse der gemeinsamen Forschungsarbeit wurden jetzt im Fachjournal „Pharmaceuticals“ publiziert (DOI: 10.3390/ph14040325).
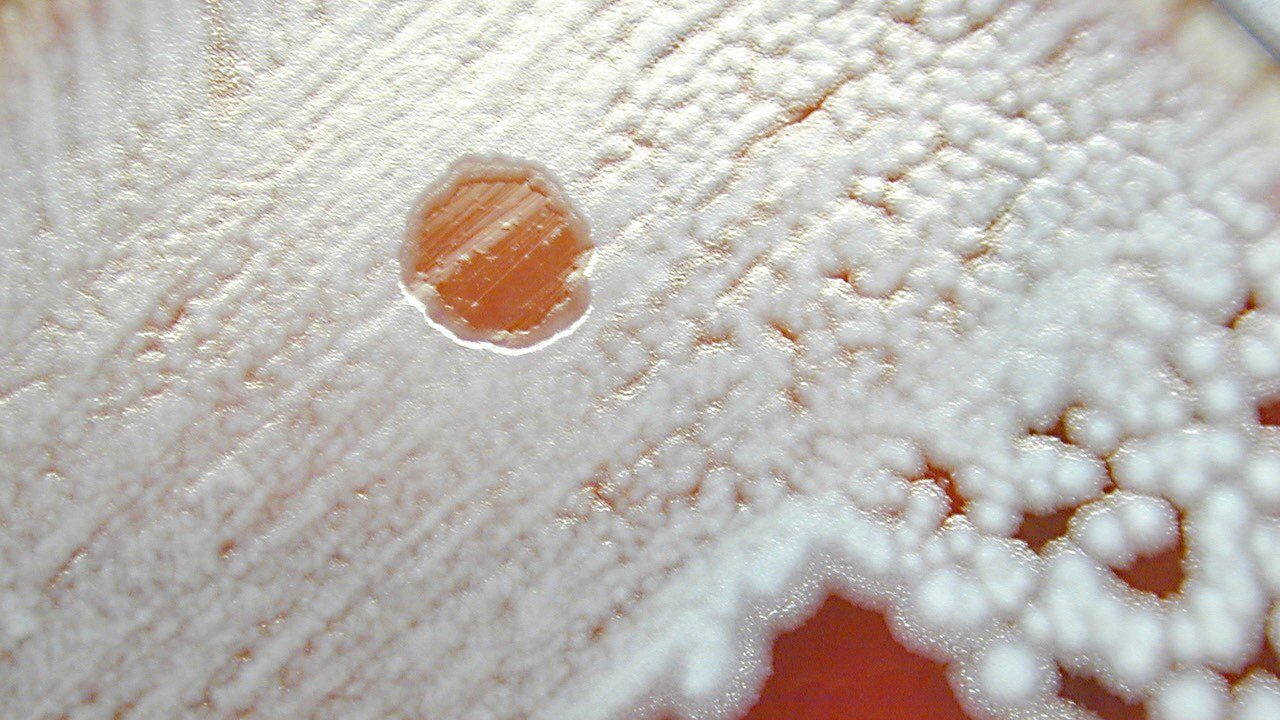
„ε² – Evolution squared“, zu Deutsch etwa „Evolution im Quadrat“, so nennt das österreichische Unternehmen PhagoMed Biopharma ihre Züchtung von „bakterienfressenden“ Viren zur Bekämpfung von Methicillin-resistenten Staphylokokken (MRSA). Eine Therapie mit den sogenannten Bakteriophagen gilt schon seit einiger Zeit als aussichtsreiche Option zur Therapie von schwer zu behandelnden Infektionen mit multiresistenten Bakterien. Sie wirken viel gezielter auf die krankheitsverursachende Bakterienspezies und können typische Resistenzmechanismen von Bakterien umgehen. Besonders auf Biofilmen – eine Art schützender Schleim, den Bakterien um sich bilden – bleiben Phagen oft deutlich besser wirksam als Antibiotika.
Hohe Spezifität großer Nachteil
Doch die hohe Spezifität der Phagen war bislang auch ihr größter Nachteil: „Bakteriophagen sind derart exakt an ihr Wirtsbakterium angepasst, dass selbst eng verwandte Stämme der gleichen Bakterienart nicht mehr von ihnen angegriffen werden. Bislang versuchte man das durch eine geschickte Mischung natürlich vorkommender Phagen zu umgehen. Selbst in günstigen Fällen wirkt diese Phagen-Mixtur oft nur bei der Hälfte aller Zielbakterien und im schlimmsten Fall wirkt er nur auf einen einzigen Stamm von hunderten“, erläutert der InfectoGnostics-Forscher Prof. Ralf Ehricht, der mit seinem Team vom Leibniz-Institut für Photonische Technologien Jena und der Friedrich-Schiller Universität Jena an der Studie beteiligt war.
Originalpublikation
Sáez Moreno, D.; Visram, Z.; Mutti, M.; Restrepo-Córdoba, M.; Hartmann, S.; Kremers, A.I.; Tišáková, L.; Schertler, S.; Wittmann, J.; Kalali, B.; Monecke, S.; Ehricht, R.; Resch, G.; Corsini, L. ε2-Phages Are Naturally Bred and Have a Vastly Improved Host Range in Staphylococcus aureus over Wild Type Phages. Pharmaceuticals 2021, 14, 325. DOI: 10.3390/ph14040325
Gezüchteter Bakteriophagen-Cocktail wirkt gegen mehr als 100 Bakterienstämme
Um optimal für den therapeutischen Einsatz geeignete Viren heranzuzüchten, nutzten die Entwickler von PhagoMed die Mechanismen der Evolution: Sie kreuzten verschiedene Phagen und selektierten diejenigen, die ein möglichst breites Spektrum an Bakterienstämmen angreifen konnten. Gemeinsam mit den Jenaer Campusforschern und weiteren Partnern testeten sie eine Mischung der so gezüchteten Phagen an 110 Staphylokokken-Stämmen. Diese Bakterienstämme hatten die Forscher vorab ausgewählt und umfassend analysiert – 43 Prozent von ihnen waren bereits multiresistente MRSA-Varianten. Das Resultat nach der Behandlung mit den gezüchteten Phagen: Bei 101 der 110 Bakterienstämme wurde das Wachstum erfolgreich unterbunden.
„Das ist ein großer Fortschritt für die Phagentherapie, wodurch sie bei manchen Krankheitsbildern als ernsthafte Alternative zur antibiotischen Behandlung von MRSA-Infektionen in den Fokus rückt“, bewertet Ralf Ehricht die Ergebnisse der Studie.
Unternehmen arbeiten an Lösungen für leichtere Analyse
Weitere Partner des InfectoGnostics Forschungscampus Jena arbeiten darüber hinaus bereits an der Gen-Analyse von Bakteriophagen: So hat das junge Startup-Unternehmen Nanozoo bereits gemeinsam mit akademischen Campuspartnern des Universitätsklinikums Jena und der Friedrich-Schiller-Universität Jena ein neues Bioinformatik-Tool namens „What the Phage“ entwickelt, das erstmals eine nutzerfreundliche Analyse von Gensequenzen von Phagen ermöglicht. Mit dem kostenlosen Open-Source-Programm lassen sich Phagen in Sequenzdatensätzen identifizieren, die sich auch für eine therapeutische Anwendung gegen passende Wirtsbakterien eignen könnten.
Mehr zum Thema Viren und Bakteriophagen, auch zum Einsatz in der Zahnmedizin, bot der Vortrag von Prof. Dr. Karin Mölling auf dem Deutschen Zahnärztetag 2019. In einem Videointerview gab sie dazu Auskunft: „Phagentherapie: Wie Viren gegen Bakterien helfen“
Weitere Beiträge:
• „Bakteriophagen – eine Alternative zu Antibiotika?“
• „Synthetische Phagen mit programmierbarer Spezifität“